原子層沉積製程技術於能源材料之應用
Applications of Atomic Layer Deposition on Energy Materials
近年來隨著地球資源過度開發以及全球暖化加劇,開發再生且乾淨並能持續使用之再生能源受到廣泛的重視,本研究團隊利用原子層沉積 (atomic layer deposition, ALD) 技術具有極佳覆蓋率並可在奈米尺度下準確控制厚度等特點,製備及修飾能源材料,應用於光電化學水解產氫以及鋰離子電池。初步研究結果顯示 經由 ALD 製備及修飾之能源材料其效能皆有所提升。
Developments of clean, renewable and sustainable energy have been received more attentions due to the limited natural resources and serious global warming in earth. In this study, atomic layer deposition (ALD) with excellent coating conformity and precise thickness control in atomic scale is proposed to fabricate and modify energy materials, applying for photocatalytic water splitting for hydrogen generation and lithium ion battery. Preliminary study shows that the performances of the energy materials are improved.
一、前言
自十九世紀工業大革命後,全球能源大幅仰賴煤、石油、天然氣等石化燃料,也因大量地使用,石化燃料經估計將於五十年內耗盡(1),此外,石化燃料在產生能源的燃燒過程中,會釋放大量有害氣體毒害環境並加劇地球暖化,因此現今尋找乾淨、可循環之替代能源是刻不容緩的課題。其中,氫氣比起化石燃料具高能量密度 (氫氣:120 MJ/kg、汽油:46.4 MJ/kg、液化天然氣:54.4 MJ/kg(2)),經燃燒後之副產物為水,為一乾淨且具有潛力的能源,更被視為取代現今石化燃料的重要選項。現今商業產氫的方式,多數仍使用石化燃料,此方式依舊會釋放二氧化碳造成地球暖化。
1972 年 Fujishima 和 Honda 發現單晶二氧化鈦經氙燈照射,進而分解水產生氫氣,開啟光電化學的大門(3),除二氧化鈦外有許多類似的半導體材料具有此特性,如:氧化鐵(4),氧化銅(5) 等但現今整體產氫效率依舊還有極大的努力空間,上述之反應過程為所謂的光催化,透過半導體以及太陽光分解水產生氫氣,其機制可由圖 1 簡略說明之(6),當半導體材料吸收大於其能隙的光源,會產生電子、電洞對,此電洞對會同時產生如圖 1 所示之 A、B、C 與 D 四種反應,A 與 B 為產生之電子、電洞分別與吸附於半導體表面之水分子或者汙染物產生氧化還原,進而產生氫氣亦或者降解汙染物。在此同時,也會產生 C 與 D 反應,分別為電子、電洞對之表面與內部之再結合 (recombination),此兩項再結合會降低電子電洞濃度而抑制光催化效能,因此,由此機制看來,若能提升 A 與 B 反應之效率 (及增加電子、電洞之濃度),降低 C 與 D 反應之效率 (降低再結合之機率),即可增加光催化水解產氫之效果,提升 A 與 B 可透過製備奈米管增加吸光強度與表面積來達成,而降低 C 與 D 之反應可經由利用氧化物以及金屬修飾半導體奈米管之表面,若要完成上述兩種策略,依照傳統鍍膜方式有諸多缺點,例如若使用溶膠、凝膠法均勻鍍覆基材,其表面有極佳親水性;濺鍍法沉積則是對於表面起伏較大、高深寬比的材料,階梯覆蓋率 (step coverage) 不佳。化學氣相沉積則是屬於擴散鍍膜機制,在起始物濃度高處,沉積較快,離起始物遠處則較慢,導致均勻性、階梯覆蓋率不佳。因此,為了克服上述缺點,將採用原子層沉積技術來製備奈米管以及沉積不同形貌、尺寸可控制之氧化物、金屬於奈米管上。
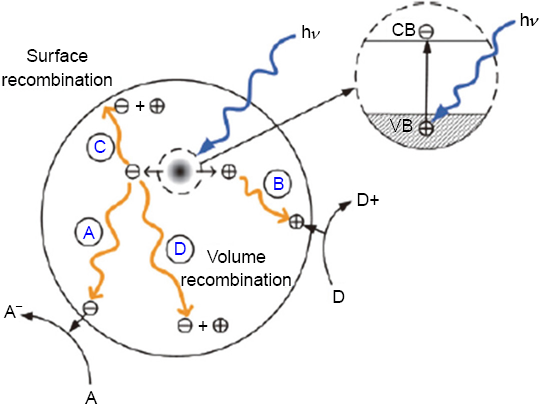
圖 1. 光催化機制(6)。
二、ALD 原理
基本上,ALD 與 CVD (chemical vapor deposition) 類似,若 CVD 全反應方程式製備 CD 薄膜以式 (1) 表示:
CY2(g) + DZ2(g) → CD(s) + 2YZ(g) (1)
不同於 CVD 沉積過程,ALD 反應為將前驅物分批且連續地注入製程真空腔體內,與基板進行交換反應 (exchange reaction),其反應可將 (1) 拆解為如下:
CY*(s) + DZ2(g) → CDZ*(s) +YZ(g) (2)
DZ*(s) +CY2(g) → DCY*(s) + YZ(g) (3)
如圖 2(a) 所示,首先通入DZ2(g) 會與基板表面官能基形成單層的中間產物 DZ*(s),待表面官能基完全反應覆蓋 DZ*(s),則達飽和, DZ2(g) 不再與基板反應 (圖 2(b)),接著進行通入惰性氣體 (purge) 或者抽氣動作 (pump) 將未反應 DZ2(g) 與副產物 YZ(g) 移除,其次,通入第二前驅物 CY2(g) 與表面中間產物 DZ*(s) 進行交換反應 (圖 2(c)),CY*(s) 完全覆蓋表面後則形成單層 (monolayer, ML) 的 CD 薄膜 (圖 2(d))。以上四步驟稱為一個 ALD 循環 (cycle),重複上述循環即可成長所需厚度之薄膜。由上述機制來看 ALD 是一種自我侷限成長,若為ALD成長之薄膜,其成長速率受溫度及氣體流量的影響不大,其成長速率與溫度的關係如圖 3 所示(7);若溫度過低,反應物凝結 (L1) 會造成有較高的成長速率,或是需要活化能 (L2) 進行相互反應,產生類似化學氣相沉積的表面自我侷限機制;若溫度過高,反應物會裂解而導致沉積速率增加 (H1),或是生成物的再蒸發 (H2) 也會使得成長速度產生變化。因此,必須選定適當反應溫度範圍 (W) 進行 ALD,此範圍稱為 ALD window,其成長速度為定值,與反應物壓力及通量無太大關係。
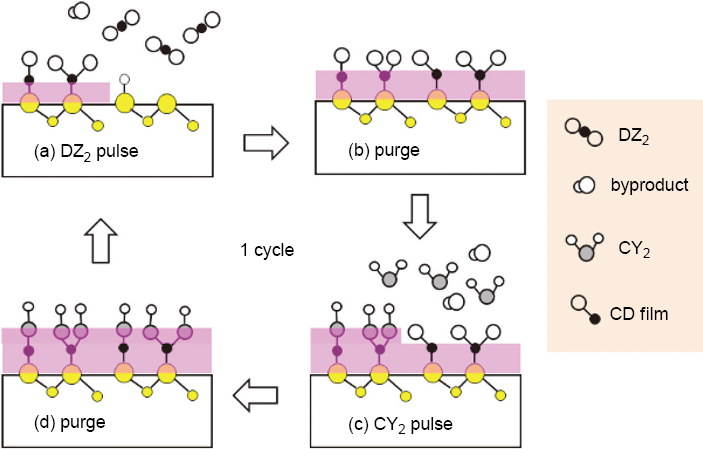
圖 2. ALD 製程示意圖。
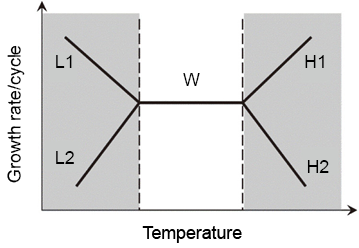
圖 3. ALD 對溫度的關係(7)。
三、ALD 於製備氧化物奈米管
由上述 ALD 基本的製程原理得知,ALD 具有極佳的取向性、均勻性且厚度能在奈米尺度下控制,因此,可利用此製程並配合奈米模版來製備所需奈米管,例如:利用有機奈米線 GaQ3 為模板沉積 ALD 氧化鋁、二氧化鈦隨後經由低溫熱處理或溶劑將有機奈米線移除獲得氧化鋁、二氧化鈦之奈米管,此厚度可利用循環數準確控制(8, 9);使用高深寬之陽極氧化鋁模板所製備之二氧化鈦奈米管陣列(10),循環數達到四百圈可得到最佳光催化效果,原因是由於此尺寸具有最佳體表面積、溶液滲透表面張力以及吸收係數,當循環數達到八百圈時奈米線則可獲得;利用 ALD 奈米層狀堆疊製程 (nanolamination process) 可用來製備複合奈米管,其複合材料之比例及管徑厚度也可準確控制,例如使用 PC(polycarbonate) 當作模版,可製備出鋅與鋁摻雜之二氧化鈦奈米管結構(11, 12),由圖 4(a) 和 (c) 可看出,雖然氧化鋅、氧化鋁對於二氧化鈦的溶解度不佳,但經由 ALD 的奈米沉積可使鋅與鋁原子均勻分布於二氧化鈦晶格之中,兩者於二氧化鈦之最大之溶解度可達 8 at%,此原因是由於在奈米尺度下表面能效應產生之現象,測試兩者之光催化水解產氫之效能 (圖 4(b) 及 (d)),結果顯示催化效果隨摻雜鋅濃度上升而上升,最大值為摻雜 1 at% 鋅,其原因為此樣品具有最多之表面氧缺陷,而摻雜鋁之二氧化鈦奈米管光催化效果隨摻雜鋁之濃度上升而急遽下降,則是由於產生過後之表面氧化鋁鈍化層所導致(13)。
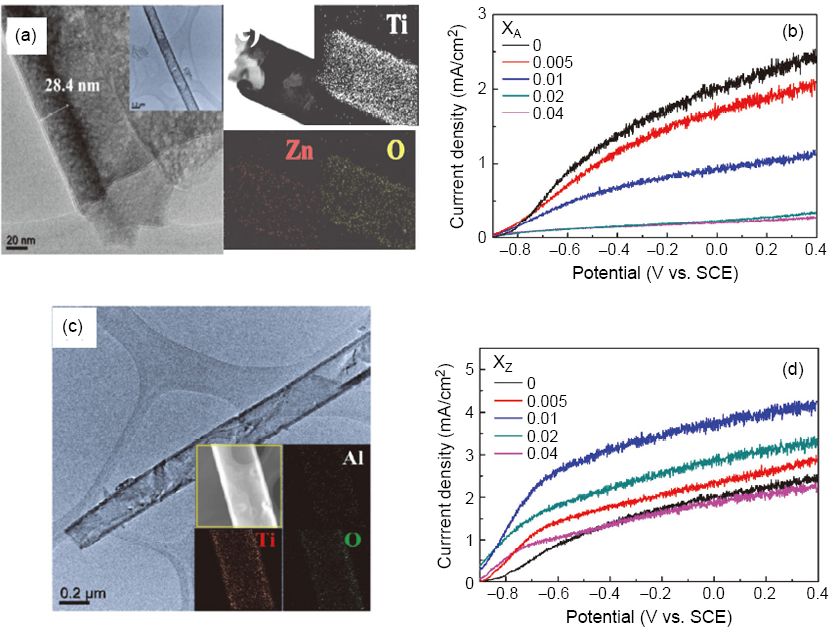
圖 4. 利用 ALD 製備 (a) Zn-doped TiO2 奈米管之 SEM 圖和其 EDS-Mapping(11) (b) 不同Zn 摻雜濃度 TiO2 奈米管之光電流(13) (c) Al-doped TiO2 奈米管之 SEM 圖和其 EDS-Mapping(12) (d) 不同 Al 摻雜濃度 TiO2 奈米管之光電流(13)。
四、ALD 於修飾氧化物奈米材料
ALD 具有極佳鍍膜覆蓋性與精準厚度控制等特點,但由於金屬薄膜前軀物取得不易,且前軀物於基板上反應性差,因此現今 ALD主要以製備氧化物薄膜為主,此高品質薄膜廣泛應用於半導體產業,例如沉積超薄高介電薄膜、金屬電極與擴散阻障層(14, 15),在能源材料的修飾上較少使用此技術;光催化奈米材料中為了減緩電子、電洞再結合機率,因此許多團隊嘗試使用氧化鋅修飾二氧化鈦減緩電子、電洞再結合提升光催化效能(16, 17)。歸咎主要原因為二者價帶與導帶的位置差異,(氧化鋅的價帶 (-7.17 eV)、導帶 (-3.8 eV) vs. 二氧化鈦(-7.6 eV)、(-4.4 eV))(16),因此當此複合材料吸收大於能階之能量產生電子、電洞分離時,氧化鋅導帶上的電子會遷移到能量較低二氧化鈦的導帶;而二氧化鈦價帶上的電洞會移動到氧化鋅的價帶,可導致電子電洞較有效分離,使二氧化鈦光催化活性有所提升,但此種方式雖可稍微提升電子、電洞分離,但效率依舊不令人滿意,最可能原因是氧化鋅的能階位置無法準確與二氧化鈦做匹配以及沉積之均勻性,因此控制氧化鋅尺寸、表面形貌、均勻性為要緊之事。因此本團隊利用氧化鋅 ALD 來修飾高深寬比二氧化鈦奈米管陣列(18),由圖 5 可得知沉積氧化鋅厚度可利用循環數準確控制,當達 200 次循環之氧化鋅 ALD,奈米管則將填滿氧化鋅形成二氧化鈦氧化鋅之複合奈米線,從 STEM-EDX 得知氧化鋅可均勻包覆高深寬比二氧化鈦奈米管 (圖 5(e)),經沉積不同厚度氧化鋅後,沉積 42 奈米氧化鋅於二氧化鈦奈米管具有最佳光催化水解產氫之光電流 (圖 6(a)),原因是由於在此時有最多可反應之載子濃度和可見光轉換效率 (圖 6(b) 及 (c))。除上述利用 ALD 薄膜修飾光觸媒材料,本團隊突破ALD製備薄膜之傳統框架,發展出奈米粒子 ALD 製程,製備光催化水解產氫所需 Pt 奈米粒子(19),此舉可有效減緩電子、電洞再結合機率,並有效強化光催化效果,其製備如方程式 (4) 及 (5) 所示(20):
Pt(s) + O2(g) → Pt-Ox(s) (4)
MeCpPtMe3(g) + Pt-Ox(s) → Pt(s) + CO2(g) + H2O(g) + other byproducts (5)

圖 5. 利用氧化鋅 ALD 沉積 (a) 50 (b) 100 (c)150 (d) 200 循環於二氧化鈦奈米管陣列之 SEM 影像及其 (e) TEM-EDX mapping(18)。
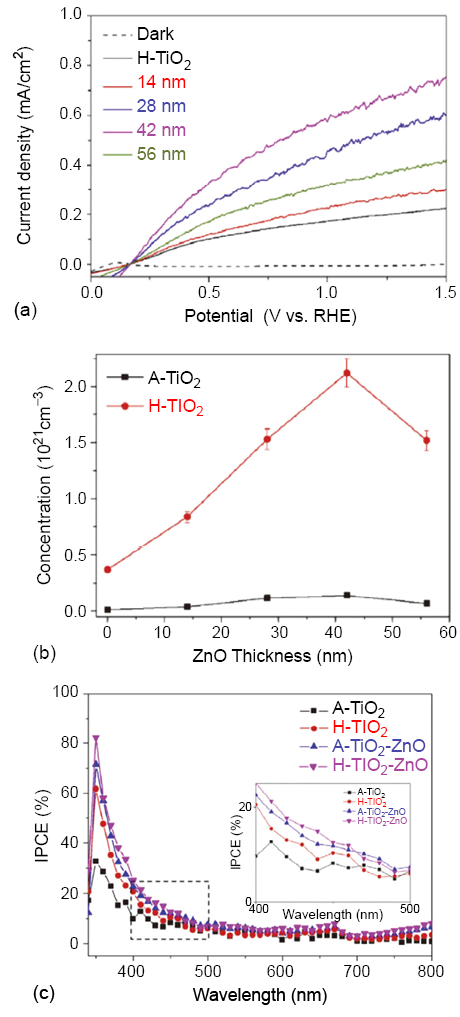
圖 6. 不同氧化鋅沉積於原始二氧化鈦 (A-TiO2) 以及氫化二氧化鈦奈米管 (H-TiO2) 陣列之 (a) 光電流 (b) mott-schottky plot (c) 光電轉換效率圖(18)。
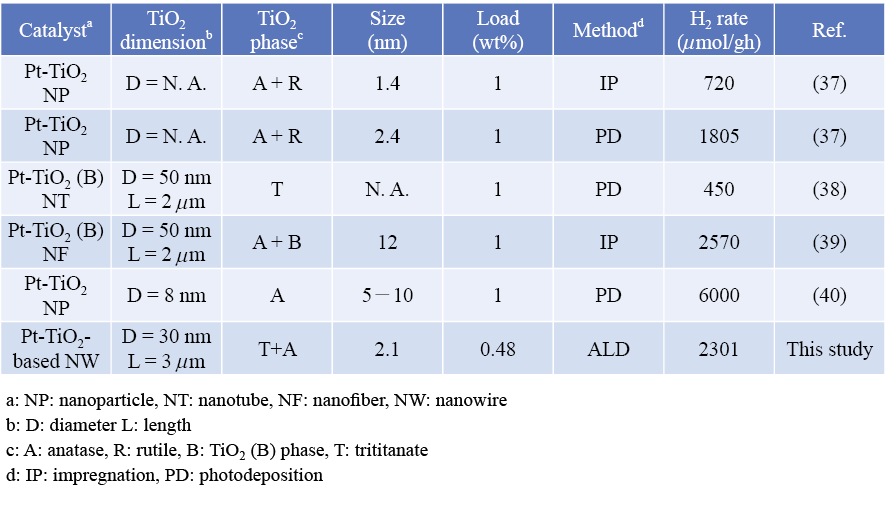
其中 MeCpPtMe3(g) (Trimethyl (methylcyclopentadienyl) platinum CAS # 94442-22-5) 為 Pt 之有機前驅物,將此白金奈米顆粒沉積於一維二氧化鈦奈米線(19),結果顯示將奈米線表面進行酸化處理及控制循環數,可獲得分散性極佳並且大小、沉積量可控制之 Pt 奈米顆粒 (圖 7),將其進行水解產氫測試發現 0.48 wt% 沉積量之白金奈米顆粒在一小時內可產出 2301 mmoles/g 的氫氣,與其他方法 (如沉浸法、光沉積法) 來相比具有較低沉積量又可得較多產氫量 (表 1),但產氫量較以二氧化鈦奈米顆粒為基材來的差,原因可能是此實驗用的是僅具少量二氧化鈦金紅石相所導致。為了降低電子、電洞再結合的機率,許多團隊在二氧化鈦上沉積白金如剛剛所述,也有利用 Au 及 Pd 等貴金屬(21-23),將其沉積於二氧化鈦的表面,由於這些貴金屬功函數 (PtΦ = 5.7 eV,AuΦ = 5.3 eV,PdΦ = 5.6 eV) 較二氧化鈦 (5.1eV) 高,當二氧化鈦接受高於能階的能量時,電子、電洞產生分離,二氧化鈦的電子會不斷的向金屬遷移,而在半導體的能帶就會向上彎曲,在表面形成耗盡層,此種在金屬與半導體界面上形成的能障稱為 Schottky 能障。電子被激發後向金屬遷移被 Schottky 能障所捕獲,使電子、電洞分離,再結合的機率變小,電洞就能自由的擴散到半導體表面將表面吸附物氧化,但貴金屬價格昂貴且地球含量稀少,對未來商業化大量生產著實不是好選擇,而鎳金屬價格便宜、含量豐富且具與貴金屬相近的高功函數 (NiΦ = 5.3 eV(24)) 為極具潛力且適合取代上述貴金屬的材料,但一般塊材鎳金屬產氫活性差需要很大的過電位,因此必須將此金屬奈米化才能有效提升催化活性,例如:Liu 等人沉積 6 mole% 鎳奈米顆粒於二氧化鈦能使光催化活性有效提升(25);Yamada 等人則發現將鎳尺寸奈米化其活性有可能與白金相近(26);而最近 Chen 等人則使用 0.2 wt% 的鎳奈米顆粒沉積於商用二氧化鈦 P25,所得水解產氫效率較沉積 2 wt% 金的二氧化鈦佳(27);雖有上述文獻描述鎳奈米顆粒能有效提升光催化水解產氫效能,但仍占少數,其原因可能是純鎳金屬的不易合成,在過程中易形成氧化物;再者,要使水解產氫效率達理想化,必須控制沈積金屬粒子之尺寸、沈積量和在二氧化鈦表面的均勻分佈。而尺寸及沈積量在文獻上未有定論也相當分歧,使用之最佳沈積量介於 0.1-6 wt% 之間,所用粒子大小多為 2-10 nm(25-27),現今最廣泛使用之鎳奈米粒子沉積方法為化學還原法、光還原法以及溶膠、凝膠法,雖然上述方法簡單,但卻無法準確嚴謹的控制上列三項要求。本團隊使用原子層沉積技術來克服上述的各項困境,以沉積尺寸、沉積量均勻的鎳奈米顆粒於黑色二氧化鈦奈米陣列使電子、電洞有效分離並獲得高產氫效率之二氧化鈦薄膜電極。與所一般所使用之鎳起始物:Ni(acac)2 (acac=acetylacetonate)(28)、Ni(dmamb)2 (damp=1-dimethyl-amino-2-methyl-2-propanolate)(29) 不同,採用新的起始物 Ni(dmp)2 (dmp=dimethylamino-2-propoxide)原因是由於此起始物經反應後有較少的不純物殘留,可能的成長機制如下:鎳起始物首先將經由極化作用與基板產生單層吸附,此時第二階段的氫氣將與之反應,而釋出配位基產生副產物形成鎳金屬,所形成的鎳金屬表面將吸附下一階段注入的氫,再與下一階段的鎳起始物產生反應,形成新的鎳金屬,如此循環作用,進行 ALD 反應(30)。
Ni(dmp)2(g) + H2 →Ni(s) + 2H(dmp)2(g) (6)

圖 7. 利用硝酸處理後之一維氧化鈦奈米管陣列沉積 (a) 10 (b) 30 以及 (c) 60 次循環之 TEM 圖以及 (d) 不同表面處理之氧化鈦奈米線對不同循環數白金 ALD 顆粒尺寸作圖(19)。
表 1. 不同 Pt-TiO2 奈米材料之產氫量比較(19)。
將此鎳奈米粒子 ALD 沉積於黑色二氧化鈦(31),所得結果顯示鎳奈米顆粒分散性佳且大小可經由循環數控制 (圖 8),成長速率與原始之二氧化鈦奈米陣列相比無差異約為 0.5 Å/cycle,當沉積鎳奈米顆粒於黑色二氧化鈦奈米管陣列有較強的光吸收光譜,原因為黑色二氧化鈦的極化效應而誘導鎳奈米粒子的電漿子共振,此材料的可見光吸收波長可隨循環數增加而往長波長偏移 (圖 9(a)),在 50 循環數時可得最佳可見光吸收強度,且具有最多的載子濃度,最後得到最佳的光催化水解產氫的性能 (圖 9(b)-(d))。
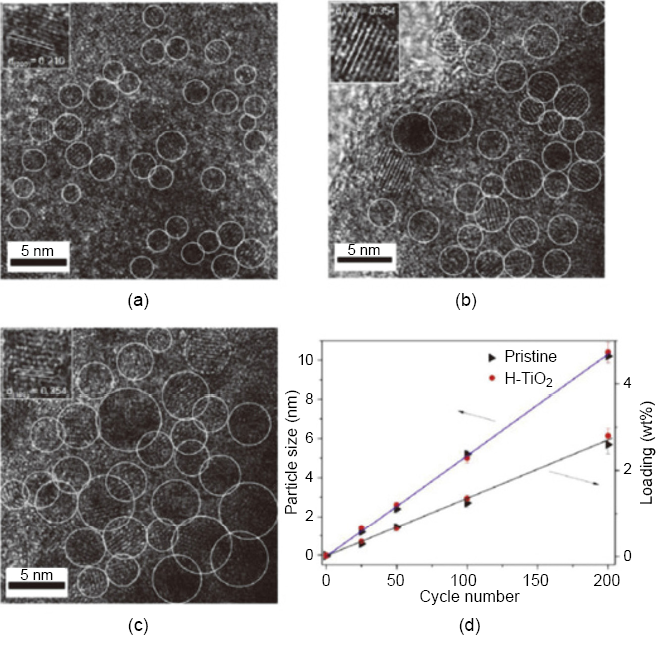
圖 8. 沉積 (a) 25 (b) 50 (c) 100 次循環之鎳 ALD 於黑色二氧化鈦奈米線之 HRTEM 以及 (d) 原始以及黑色二氧化鈦奈米線沉積不同鎳 ALD 循環數與顆粒大小和沉積量之作圖(31)。

圖 9. 不同次循環之鎳 ALD 於黑色二氧化鈦奈米線之 (a) 紫外可見光光譜 (b) 水解產氫之光電流 (c) mott-schottky plot (d) 光電轉換效率圖(31)。
五、ALD 於修飾鋰離子電池陰極材料
商用鋰離子陰極材料以 LiCoO2、LiNi1/3Mn1/3Co1/3O2 最廣泛使用,但由於此材料 Co+3/+4(3d) 軌域與 O-2(2p) 軌域相互重合,造成整個化學結構上不穩定,也造就了此材料僅僅使用約理論電容量的百分之五十(32, 33),現今所得的最高能量密度約為 150 Whkg-1,富鋰離子層狀氧化物具有最高的電容量 (~250 mAhg-1) 可以得到最高的能量密度,但若要商業化,還需克服低倍率性能及循環性缺失;最主要的原因即是充放電過程中,陰極層狀氧化物與電解質中有機溶劑產生很厚的 SEI (solid electrolyte interfaces),阻礙鋰離子擴散並影響表面導電性(34, 35) 以及電解質中少量 HF 攻擊電極表面導致活性物質失去電化學活性,因此,若要提升倍率性能,必須盡可能防止表面 SEI 層產生並阻止 HF 之直接攻擊以提昇表面導電性,現今有許多利用不同氧化物修飾鋰離子電池陰極提升倍率性能[],但甚少使用 ALD 來修飾富鋰離子層狀氧化物陰極表面,本團隊近期沉積 ALD 二氧化鈦與氧化鋅於富鋰離子氧化物陰極表面(36),結果發現兩者於此陰極表面生長機制不同,二氧化鈦為層狀生長,氧化鋅則是島狀成長機制 (圖 10),電化學效能顯示經二氧化鈦 ALD 修飾之倍率性能以及循環性能皆比氧化鋅修飾有所提升 (圖 11),其原因則是由於層狀二氧化鈦沉積於電極有較少缺陷,可完整包覆電極比起島狀成長之氧化鋅可有較完整保護,使電子、離子傳輸較為順暢。

圖 10. (a) 富鋰離子層狀氧化物以及沉積 (b) 氧化鋅和 (c) 二氧化鈦鎳 ALD 之 TEM 圖(36)。
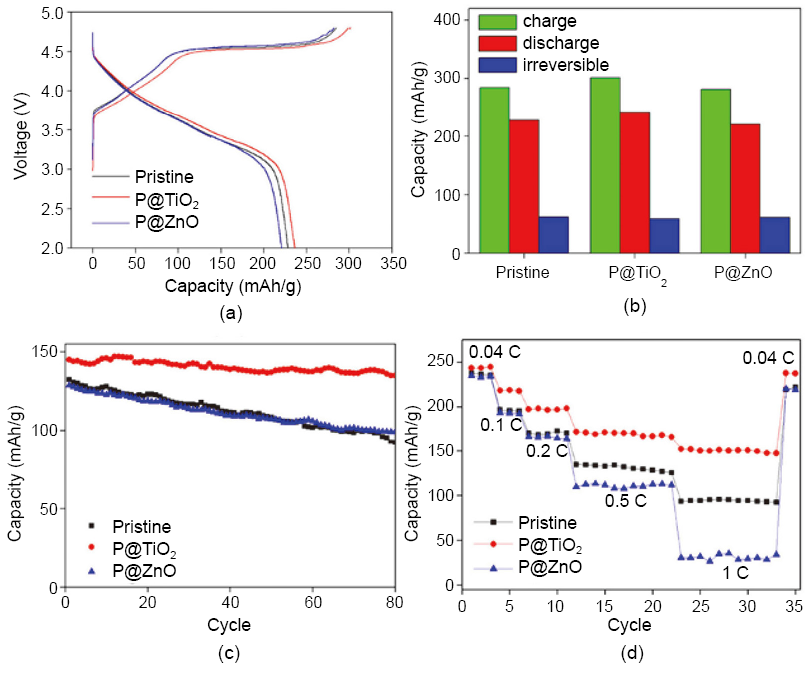
圖 11. 原始富鋰離子層狀氧化物 (Pristine) 以及沉積二氧化鈦 (P@TiO2) 以及氧化鋅 (P@ZnO) ALD 之 (a) 第一次充放電容量 (b) 第一次充、放電容量以及其不可逆電容量 (c) 循環性能以及 (d) 循環倍率性能圖(36)。
六、結論
ALD 具有極佳薄膜沉積覆蓋性與準確奈米尺度控制,可應用於製備和修飾能源材料,除在製備半導體之薄膜外,可用來製作奈米管並且控制其組成,但用來製備於奈米粒子領域仍屬少數。從研究結果得知,結合 ALD 薄膜製程與有機奈米線、AAO 以及 PC 等奈米級模板,可輕易製備光催化奈米管,增加反應比表面積,並且經由加入不同氧化物沉積可摻雜成分均勻之奈米管,提升可見光吸收率和增加表面缺陷增強光催化效率。以 ALD 白金及鎳奈米粒子修飾奈米管表面,經由調控最佳尺度、沉積量,可有效使電子、電洞再結合機率下降,光催化產氫的效果能顯著提升。此外,在儲能領域上,經由 ALD 修飾鋰離子電池陰極材料可有效保護其表面避免電解質中之 HF 攻擊以及形成過厚 SEI 層,影響電子和離子傳輸,有效提升其倍率和循環性能,此上述 ALD 在光催化水解產氫以及鋰離子電池電極上之研究,可提供未來 ALD 於不同系列能源材料應用之參考。