短波長微生物光抑制技術分析與應用
Analysis and Application of Short-wavelength Light Inhibition Technology for Virus and Bacteria
2019 年底由嚴重急性呼吸系統症候群冠狀病毒引發的特殊傳染性肺炎,於 2020 年初於全球迅速擴散,台灣醫療在歷經 2002 年 SARS 及 2009 年 A 型流感病毒 H1N1 疫情後,在政府扶植及民間投資下,針對此次新冠病毒 (COVID-19) 積極開發各項防疫技術,除了減少飛沫傳染的口罩外,消毒技術亦為發展重點,其中以光抑制方式破壞病毒結構則屬最方便且可被廣泛應用之方式。本研究開發短波長光抑制系統,並實際於第二等級生物實驗室進行病毒驗證生物測試與分析。實驗結果得知以 50 mJ/cm2 以上之光劑量照射時,對病毒有 99.99% 之抑制率。
At the end of 2019, the special infectious pneumonia caused by severe acute respiratory syndrome coronavirus that spread rapidly around the world in early 2020. After the 2002 SARS and 2009 influenza A virus H1N1 outbreaks in Taiwan, Taiwan᾿s medical treatment was supported by government support and private investment. For the new coronavirus (COVID-19), actively develop various anti-epidemic technologies in Taiwan. Therein, the masks is a necessary object which can reduce the infection of droplets, and the disinfection technology is also the focus of development. Among them, the use of light suppression to destroy the virus structure is the most convenient and can be widely used and applied in our life. This research develops a short-wavelength light suppression system and actually conducts a biological testing for virus verification in Biosafety level 2 environment (P2 Lab). The experiments show that when the virus of 229E was irradiated with a light dose of 50 mJ/cm2 or more, the virus has a 99.99% inhibition rate.
一、前言
2019 年 12 月起,經由少數個案病患的呼吸道疾病與相關疾病監測,發現不明原因的病毒性肺炎,其臨床表現主要有發燒,少數病患則有呼吸困難,經由胸部 X 光則可發現雙肺呈浸潤狀態。經由電子顯微鏡下觀測,可看到病毒外表呈圓形,並具有類似皇冠的突起,呈現典型冠狀病毒型態。國際病毒分類學會將此病毒學名定為 SARS-CoV-2 (Severe Acute Respiratory Syndrome Coronavirus 2),屬冠狀病毒科 (Coronavirinae) 之 beta 亞科(betacoronavirus),為一種具有外套膜的單股正鏈 RNA 病毒(1),人類感染冠狀病毒通常以咳嗽、鼻塞、流鼻水、發燒等一般上呼吸道症狀為主,但若是感染嚴重急性呼吸道症候群冠狀病毒 (SARS-CoV)、中東呼吸症候群冠狀病毒 (MERS-CoV) 與新型冠狀病毒 (SARS-CoV-2)後會比一般人類冠狀病毒症狀嚴重,部分病患可能會出現嚴重的肺炎與呼吸衰竭等症狀,世界衛生組織 (World Helth Organization, WHO) 亦將此新型冠狀病毒造成的疾病稱為 COVID-19 (Coronavirus Disease-2019),其臨床症狀除發燒、乾咳、倦怠外,還會有呼吸急促、頭痛、肌肉痛、喉嚨痛、腹瀉,甚至喪失味覺或嗅覺。經由全球疫情的快速發展,世界衛生組織更宣布此次疫情已構成全球大流行,其中依據 European CDC 調查與統計指出,此次傳染病開始的五個月後,於美國、俄羅斯等國家,每一百萬人的確診人數更高達 5000 人以上 (如圖 1)。根據臨床病症與實驗室檢測結果,藉由近距離飛沫、間接或直接接觸帶有病毒的口鼻分泌物,或與無任何呼吸道防護下之確診病人處於 2 公尺之密閉空間裡,將增加人傳人之感染風險,其中感染新型冠狀病毒之發病潛伏期為 1 至 14 天,主要在發病的前兩天會具較高的傳染力,而從病人的上呼吸道檢體的核酸檢測結果可發現,呈陽性之時間平均達兩週以上,因此,為減少新冠病毒感染機會,可針對病毒飛沫傳染之特徵著手進行預防,避免出入人潮擁擠、空氣不流通之公共場所,配戴口罩或維持一定社交距離,並維持手部清潔,減少觸碰眼口鼻,以避免直接或間接接觸帶有病毒之分泌物。
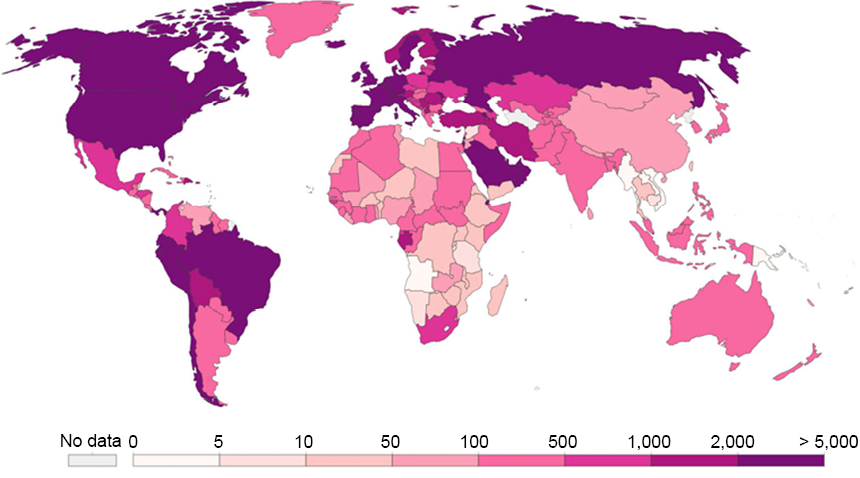
圖 1. 2020 年五月底全球每百萬人之確診人數統計分佈圖 (資料來源:European CDC)。
新型冠狀病毒為一種具有包膜、且被宿主細胞提供的脂質雙層包裹的不分節段正鏈單股 RNA 病毒,其中含有核酸與核衣殼蛋白,形狀主要為圓形或橢圓形,直徑長度約 80-120 nm。依據對病毒的實驗結果顯示,病毒具有熱敏感性,在空氣或物體表面可以長時間存活,其中在室溫環境下可存活長達 9 天,而在不同材質組成的表面保持感染性時間則有 2 小時至 9 天不等,根據美國國家衛生研究院 (National Institutes of Health, NIH) 的病毒學家於新英格蘭醫學雜誌(2) 上發表的研究結果顯示,SARS-CoV-2 病毒在銅的表面約可存活 4 小時,在硬紙板上可存活達 24 小時,而在不鏽鋼或塑料表面的存活時間可達 2-3 天。以光學或熱能之物理機制而言,提升冠狀病毒所在環境的溫度有助於殺死病毒,但溫度與時間成為重要的參數,在高於 56 °C 的環境,每 15 分鐘僅能殺死一萬個病毒顆粒,因此即使在 60 °C 的環境下,病毒也還有些微的繁殖能力,要將其暴露在紫外線下達到特定劑量或將其放置於 92 °C 的環境中長達 15 分鐘以上,才能有效抑制病毒的活性。
此外,以化學方式可以更快的殺死病毒,其中因新型冠狀病毒的外套膜含有酯類,而酒精可以溶解酯類,因此酒精可以使病毒失去活性,而次氯酸 (hypochiorous acid,化學式 HCIO) 的氧化能力亦能破壞蛋白質結構,因此具有次氯酸成分的漂白水或次氯酸水也可以抑制病毒的活性,其中上述三種物質最佳的濃度為:濃度 75% 的酒精、0.5% 的雙氧水漂白劑或 0.1% 的次氯酸鈉漂白劑,都可以在一分鐘內對新冠病毒進行消毒。而肥皂或清潔劑,因能帶走油脂,因此也可藉由勤洗手的方式減少病毒殘留的機會。然而,上述三種化學物質的消毒方法(3),各有其優缺點,其中酒精具有攜帶與設置方便且揮發快速的優點,因此可以作為無法濕洗手消毒時的替代方式,而漂白水則容易刺激眼睛、口鼻及皮膚,接觸太久可能造成灼傷,因此建議用來進行環境消毒,使用時盡量減少採用噴霧以避免刺激呼吸道,並戴上手套以擦拭方式進行消毒,且漂白水建議於稀釋泡製後的 24 小時內使用完畢以維持其消毒效果。而次氯酸水的刺激性雖低於漂白水,但其仍對皮膚與粘膜有刺激性,因此亦較建議用在環境清潔,避免用於人體消毒,同時氯酸水的保存要盡量減少與空氣接觸、加上不耐日光與高溫,故須保存於不透光的陰涼環境。
表 1. 各式紫外線比較表。
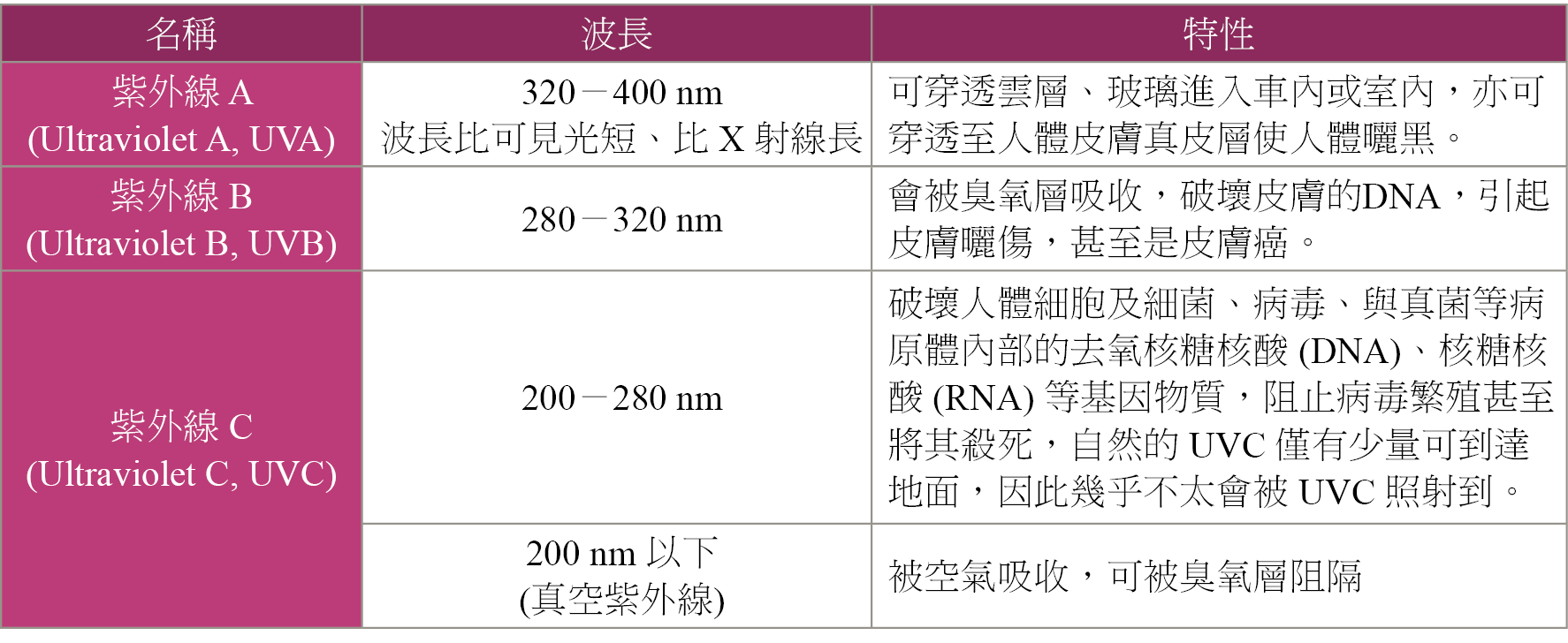
雖然以化學方式可快速針對病毒活性進行抑制,然有多數物品是無法進行濕式消毒的,因此,以乾式消毒的之儀器設備亦成為防疫期間相關設備的研發重點。本研究主要建構以光的機制進行病毒活性抑制之儀器設備,並進行活性抑制分析探討。其中一般常見以紫外線進行消毒,其具備殺菌面積廣、使用方便、價格低廉、可重複使用、應用範圍廣等優點。然而紫外線 (ultraviolet, UV) 又可以依其波長分佈範圍分為好幾大類,其波長比可見光短、又比 X 射線長,主要波長介在 320-400 nm 的為紫外線 A (UVA),可穿透雲層、玻璃進入車內或室內,亦可穿透至人體皮膚真皮層使人體曬黑。波長介於 280-320 nm 之間的紫外線 B (UVB),會被臭氧層吸收,並會破壞皮膚的 DNA,引起皮膚曬傷,甚至是皮膚癌。而波長介於 100-200 nm 的則為紫外線 C (UVC),其中又將波長 200 nm 以下定義為真空紫外線,會被空氣吸收,可被臭氧層阻隔,可穿越大氣層的紫外線 C,波長主要介於 200-280 nm 之間,可以破壞人體細胞及細菌、病毒、與真菌等病原體內部的去氧核糖核酸 (DNA)、核糖核酸 (RNA) 等基因物質,阻止病毒繁殖甚至將其殺死,但因為自然的 UVC 僅有少量可到達地面,因此我們幾乎不太會被 UVC 照射到,因此現在大多以低壓汞燈的方式來發出 UVC 波長的光,其主要的波長會有 253.7 nm 與 185 nm 兩個峰值,其中波長 185 nm 的紫外線可產生臭氧,亦可作為除臭、除菌、抑霉等使用。雖然每個人對於紫外線的容忍度都不相同,但是只要累積到一定程度,都會造成損傷,而且不管是 UV-A/B/C,都會對眼睛與皮膚有所傷害,導致皮膚癌或眼睛白內障等問題,因此在使用紫外光時,都要盡量避免直視與直曝光源下。
此外,2017 年哥倫比亞大學醫學中心的 David Brenner 教授的研究(4) 曾提出,波長 222 nm 以下的遠紫外光 C (Far UVC) 可殺死病毒與細菌,但無法穿透人類的眼睛淚膜與皮膚死皮層,因此對人體無害,其研究結果亦同步顯示,在不傷害老鼠皮膚之情況下,成功消滅多重抗藥性之金黃葡萄球菌。然在波長 222 nm 的紫外光燈尚未普及之前,大多應用仍使用波長 253.7 nm 之 UVC 燈源作為消毒的主要光源,能提供較高之能量,減少照射所需之時間。
二、病毒效價定量介紹與應用
病毒的定量涉及在一個特定的體積中計數病毒的數目,來確定病毒的濃度。它可用於商業和學術實驗室的研發以及生產,在實驗環境中,各個步驟的病毒數量是一個很重要的決定因子。例如,生產病毒疫苗,需使用病毒定量來不斷改進和監測疫苗的生產過程。1952年,Renato Dulbecco 把噬菌體空斑技術,應用於動物病毒學,從而使病毒空斑試驗 (plaque assay) 成為許多病毒效價 (titer) 定量和研究的方法。病毒空斑試驗類似噬菌斑的測定法,是根據感染劑量來確定病毒濃度的標準方法。病毒空斑試驗可確定病毒樣品中噬斑形成單位 (plaque-forming unit, pfu) 的數量,這是病毒數量的一種單位,該測定是基於在細胞培養皿或多孔板中進行的微生物學方法。具體而言,將細胞培養皿種滿單層宿主細胞,以不同的稀釋濃度來稀釋病毒,並將稀釋後的病毒感染單層宿主細胞,並用半固體培養基 (如瓊脂或羧甲基纖維素) 覆蓋感染病毒後的宿主細胞,以防止病毒感染肆意傳播。當病毒感染固定細胞單層內的細胞時,會形成病毒空斑。被病毒感染的細胞將裂解,並將病毒傳播到鄰近的細胞,在該細胞中重複進行感染-裂解細胞的週期。受感染的細胞區域將形成一塊空斑,可以通過光學顯微鏡或肉眼觀察到,倒出半固體培養基並加入結晶紫溶液 15 分鐘,直到其對細胞質著色,用水輕柔地去除多餘的部分,死細胞的位置顯示無色。空斑塊的形成,根據不同病毒可能需要 3 到 14 天,取決於所分析的病毒。通常以手動計數病毒空斑,計算每單位樣品體積的病毒空斑 (pfu/mL)。病毒定量單位 pfu/mL 基於以下假設,所形成的每個病毒空斑代表一個感染性病毒顆粒,此單位代表樣品中具感染性的病毒顆粒數量。
為了進行病毒空斑測定,製備 10 倍稀釋的病毒原液,並將 0.1 mL 樣品接種到培養皿的單層宿主細胞上。溫育期過後,為了使病毒附著在細胞上,單層覆蓋半固體培養基,該培養基通常含有會造成凝膠形成的瓊脂。原始感染的細胞釋放病毒後代。新病毒的傳播受到半固體凝膠的限制。因此,每個感染性顆粒都會產生一個圓形的感染細胞區,稱為病毒空斑。最終,斑塊變得足夠大,以肉眼可見。染色活細胞的染料通常用於增強活細胞和病毒空斑之間的對比度。這樣就能定量可感染細胞的病毒數。圖 2 顯示了由 229E 冠狀病毒在 Huh7 細胞單層上形成的病毒空斑。在此圖中,細胞已被結晶紫染色,在病毒感染已破壞的單層宿主細胞的地方形成白色病毒空斑塊。
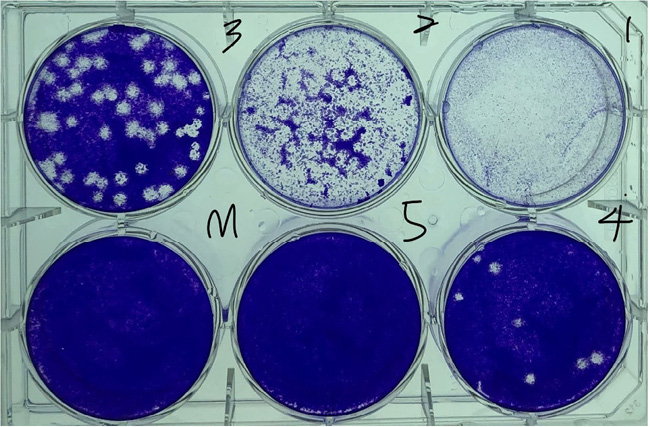
圖 2. 病毒空斑測定實驗之細胞與病毒空斑塊圖 (數字 1 至 5 以十倍稀釋)。
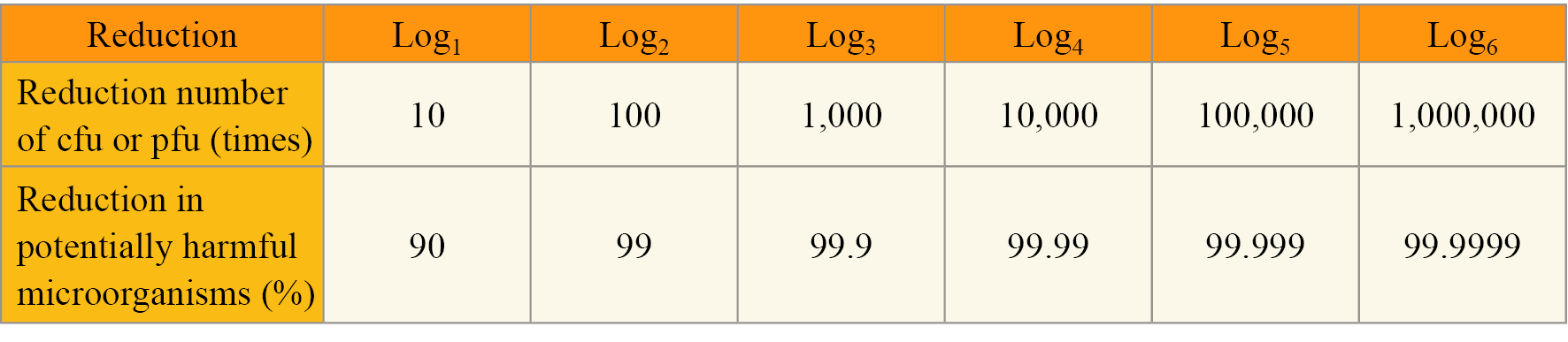
病毒原液的效價定量,可以每毫升病毒空斑形成單位 (pfu/mL) 計算。為了確定病毒效價的定量,僅計數包含 10 至 100 個病毒空斑的孔洞盤,取決於所用細胞培養板的大小。當計數 100 個病毒空斑時,病毒樣品效價定量,將產生正負 10% 的病毒空斑數量。對病毒與細菌的減少與消毒成功率定義,當 pfu (對病毒之數量計算) 或 cfu (colony forming uint,對細菌之數量計算) 之數量為十倍減少時,則定義為 1-Log 的減少 (Log1),並定義為 90% 的消毒、殺菌,當待測物表面的病毒或細菌數量自 1,000,000 (cfu/pfu) 下降 4-Log 至 100 (cfu/pfu)時,則表示潛在的有害微生物減少了 99.99%。
表 2. 細菌或病毒減少率與數量關係表(5)。
病毒空斑試驗主要應用於病毒純化與蝕斑減少中和試驗,其說明如下:(1) 病毒純化(virus purification),在進行血清中和試驗時,常常會出現標準病毒株的效價下降,因而影響了後續試驗的準確性,這種情況常見於蟲媒病毒。可能是由於原始病毒株的混雜,或已有許多變異病毒顆粒存在其中,甚至出現數量眾多的缺陷病毒所致。這時,有必要把標準毒株進行純化,應用病毒空斑試驗技術,挑選出各個不同的純化病毒,亦稱「克隆病毒株」。克隆後的病毒株經測定其病毒效價定量,來選擇合適的病毒株用於血清中和試驗。為了更有效地進行病毒株的純化,必須在覆蓋半固體營養瓊脂之前,用營養液洗去單層細胞上未被吸附的病毒。同時要控制好稀釋的濃度,一個孔洞盤的病毒空斑數目最好不超過 10 個,挑取附近 10 mm 都是健康細胞的病毒空斑。挑取後的病毒株應傳兩代或兩代以上。(2) 蝕斑減少中和試驗 (plaque reduction nutralization test),病毒空斑減少中和試驗是檢測血清中和抗體的一種敏感方法,以病毒空斑數減少 50% 的血清稀釋度作為其中的效價。使用定量的病毒 (100PFU) 與不同稀釋度的等量血清混合後,接種單層宿主細胞,再覆蓋上半固體營養瓊脂,置於 37 °C 二氧化碳培養箱培養,數天後分別統計病毒空斑數,來推測血清中是否具有中和病毒的抗體存在。
三、輻照劑量介紹
在光學裡,輻照度 (irradiance) 為電磁輻射入射於每單位面積的功率,被照物與光源間的輻照度與距離有關,並以平方反比遞減。紫外光的輻照劑量主要由輻照強度(輻照度)與照射時間的積分,其關係可以式 (1) 表示。其中 I 為輻照強度,單位為 mW/cm2,t 為照射時間,單位為 sec。因此輻照劑量為兩項參數之乘積,為單位面積下累積多少焦耳 (mJ/cm2)。當被照物體表面的輻照強度不夠時,則可以延長照射時間的方式來達到相同的輻照劑量。
K = I × t (1)
四、紫外光消毒系統介紹
市售有多項號稱為紫外光消毒系統之儀器,但是對於消毒燈源之波長、輻照強度等參數並無完整標示,甚至不一定有經過實際的消毒驗證,為此,本團隊於防疫期間,快速發展一套以紫外光燈管 (UVC) 為光源,波長為 254 nm 之紫外光消毒測試機,本測試機可於固定光源下調整樣品放置之相對距離與位置 (如圖 3),並實際測試不同位置與距離下之輻照強度,其中光學輻照度之工程參數驗證示意圖如圖 4(a) 所示,於工程參數量測完後,將本紫外光消毒測試機送至長庚大學新興病毒感染研究中心內之第二等級生物之實驗室進行病毒抑制測試,測試期間生物樣品與光源之擺放位置圖如圖 4(b) 所示,於生物測試期間,培養皿擺放於燈管光源之正下方且正中間處即圖 4(a) 之 B 點位置。

圖 3. 紫外光消毒測試機 (a) 外觀、(b) 內部燈源與樣品擺放示意圖。
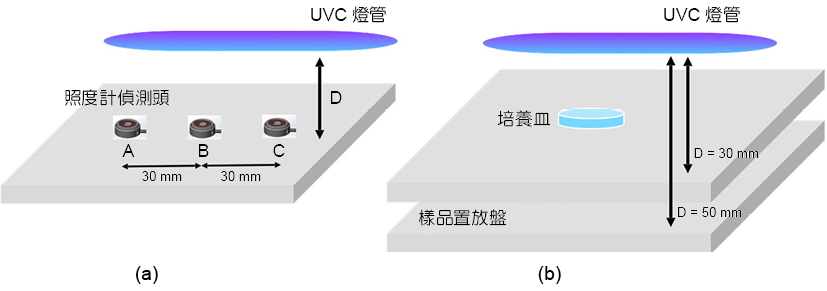
圖 4. 紫外光消毒測試機 (a) 工程參數驗證、(b) 生物消毒驗證實驗擺放配置示意圖。
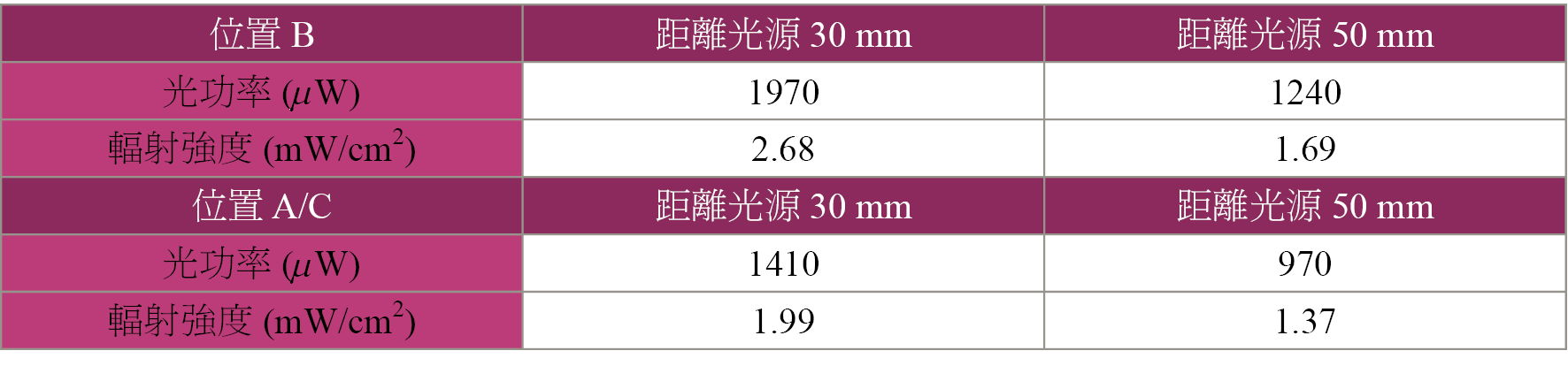
當系統架設完後,使用光功率計 (PM100D, Thorlabs) 與光功率感測器 (S120VC, Thorlabs) 距離燈管 30 mm 及 50 mm,於燈管正中間 (圖 4(a) 之 B 點) 及正中間左右距離 30 mm 的位置處 (圖 4(a) 之 A、C 點) 進行功率量測,因光功率感測器之偵測區入光直徑約為 9.5 mm,因此於正中間之位置,距離光源 30 與 50 mm下換算之輻射強度分別為 2.68 與 1.69 mW/cm2 (如表 3)。
表 3. 紫外光平均光功率與輻射強度。
根據 Eickmann 等人(6) 分析嚴重急性呼吸道症候群冠狀病毒 (SARS-CoV)、克里米亞-剛果出血熱病毒 (CCHEV) 與 Nipah 病毒 (NiV) 等三種新興病毒,於紫外光及藍光下的病毒抑制效果,發現以全 UVC 劑量 (200mJ/cm2) 的一半至四分之三的光強度進行治療時,SARS-CoV 的傳染性對數可降低 3·4 log,CCHFV 與 NiV 的傳染性對數則分別降低 2·2 log 與 4·3 log,並達到血小板濃縮液的檢測極限 (limit of detection)。依此文獻的研究結果發現,冠狀病毒之消毒劑量約在 100-150mJ/cm2。因此,估計以本系統進行消毒測試所需之時間約需大於 50 秒才能有效抑制病毒之活性。然而,實際以具備 229E 冠狀病毒之樣品放置於燈管正中間 (圖 4(a) 之 B 點),進行光照與細胞感染分析,本次實驗加入 0.5 mL 的病毒液體,在 30 mm 照射 10 秒之病毒空斑形成單位實驗圖中,可於稀釋至 104 濃度下,計算出 7 個病毒空斑 (如圖 5(b)),可換算成病毒量數為 1.4 × 105。控制組 (未照光) 及於 50 mm 距離下照射 10 秒之樣品,因光照劑量不足,較難具有消毒效果,可於稀釋至 104 濃度下發現 8 個病毒空斑 (如圖 5(a)、(d),換算成病毒量為 1.6 × 105。於距離於 30 及 50 mm 下,照射 30 秒以上即無發現病毒空白斑塊 (如圖 5(c)、(e),抑制效果在此條件下可達 99.99%。
表 4. 紫外光照射時間與病毒空斑形成單位數量統計表。

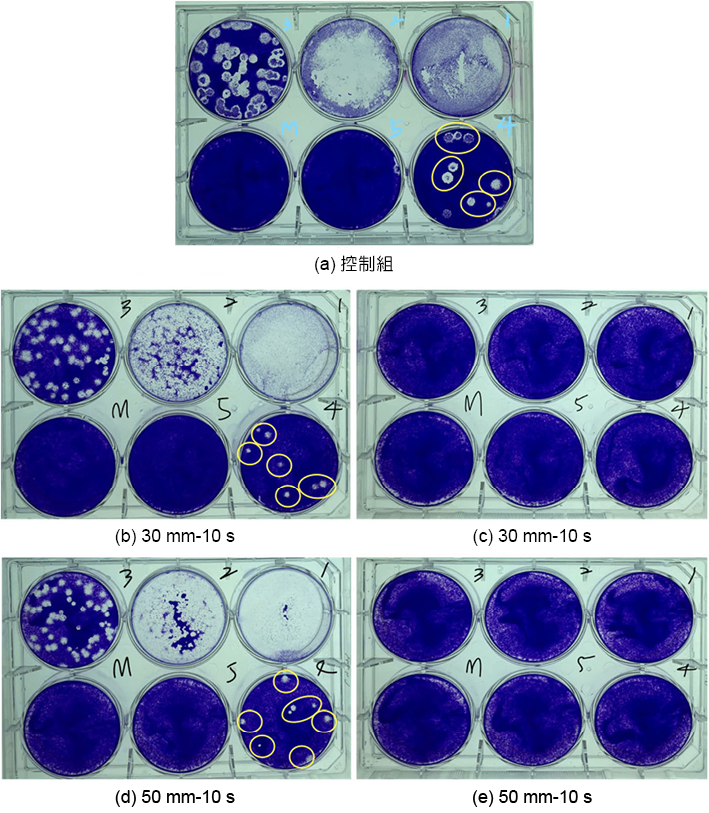
圖 5. 病毒空斑實驗圖 (a) 控制組、(b) 距離 30 mm-照射 10 秒、(c) 距離 30 mm-照射 30 秒、(d) 距離 50 mm-照射 10 秒、(e) 距離 50 mm-照射 30 秒。
根據國內外媒體對於疫情資訊之報導,可發現國外有因公文傳遞造成多人感染新冠病毒之嚴重漏洞,因此,為降低病毒可能的傳染風險,本中心將上述之研究成果實際應用,成功開發出多功能文件消毒機 (如圖 6),可針對特定厚度下之文件表面 (可被光照射之面積) 進行消毒,並以本研究之實驗數據做為機台開發設定之參數 (如照射距離、時間),本機台亦實際放置於科技部之公文收發室使用,針對每天經手之公文進行消毒,減少病毒傳染之風險。

圖 6. 多功能文件消毒機實體圖。
五、結論
本文介紹了有關新冠病毒之抑制方法,除濕式消毒法外,本研究亦開發以光機制進行病毒活性抑制之方法,並實際於第二等級生物之實驗室內,以感染症狀較輕之 229E 冠狀病毒進行光抑制測試,經由實驗結果發現,以 1.69 mW/cm2 以上之輻射照度,照射 30 秒以上,即可有效降低病毒之活性,抑制效率達 99.99% 以上,除工程系統開發、實際生物特性驗證外,亦成功將此研究之結果發展成一套多功能文件消毒機,完成工程參數測試、生物測試,到應用雛形機開發,未來,更將著重於不同之光能或熱能消毒機制之研究與應用產品研發,拓展微生物光抑制技術之應用領域,增進本技術於防疫科技領域之應用廣度與深度。